BCMA ( B 细胞成熟抗原)由位于 16 号染色体短臂的 TNFRSF17 基因编码,由 184 个氨基酸组成,分子量为 20.2 kDa ,是一种 III 型跨膜糖蛋白,包含胞外结构域( ECD )、跨膜结构域( TM )和胞内结构域( ICD ),胞外 N 末端无信号序列,含有 6 个半胱氨酸的保守基序 [1] 。在特定酶(如 γ- 分泌酶)的作用下, BCMA 的细胞外结构域被切割,释放到血液中形成可溶性 B 细胞成熟抗原( soluble BCMA, sBCMA ) [2] 。 sBCMA是 B 细胞参与人类自身免疫性疾病的潜在生物标志物。常见的自身免疫性疾病包括多发性硬化症、 N- 甲基 -d- 天冬氨酸受体 (NMDAR) 脑炎、重症肌无力、系统性红斑狼疮 (SLE) 、类风湿性关节炎、髓鞘少突胶质细胞糖蛋白谱系障碍 (MOGSD) 和视神经脊髓炎谱系障碍 (NMOSD) 。 BCMA 在正常组织中仅限于浆母细胞、浆细胞等免疫细胞表达,但在多发性骨髓瘤( Multiple myeloma, MM )等疾病中高增殖导致表达显著增加。这一特性使其成为治疗多发性骨髓瘤的理想治疗靶点。
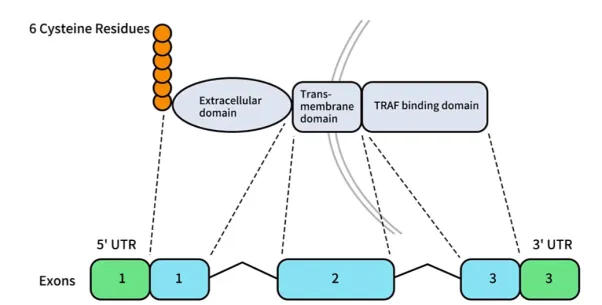
图 1 . BCMA 基因和蛋白的结构
作为靶向治疗靶点,
BCMA疗法包括嵌合抗原受体
T
细胞
( chimeric antigen receptor T - cell immunotherapy,CAR - T)
疗法、单克隆抗体疗法(包括裸抗和抗体药物偶联物
( antibody drug conjugates,ADC)
和双特异性抗体
( bispecific monoclonal antibody,BsAb)
疗法等三大阵营
[3]。
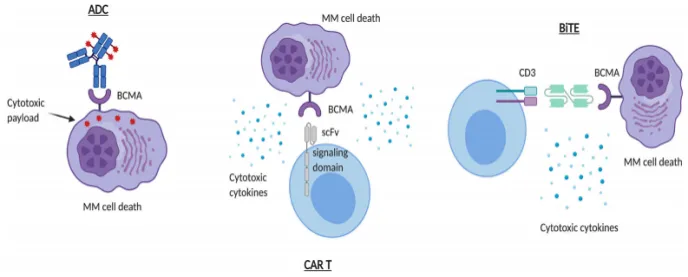
图 2. BCMA靶向免疫疗法
CAR - T疗法
CAR-T细胞疗法是将自身的 T 细胞在体外进行基因修饰后回输到患者体内进而杀死体内的肿瘤细胞。通用型 CAR-T 细胞疗法是指从健康捐献者体内分离提取 T 细胞,通过基因编辑或非基因编辑改造和体外扩增后,最后可输入多位患者体内的疗法。而以 BCMA 为靶点的 CAR -T 疗法优点在于具有结合单克隆抗体的靶点特异性和 T 细胞的细胞毒性的特点,可以不受人类白细胞抗原 ( human leucocyte antigen,HLA) 的限制 [4]。 CAR-T细胞上的 BCMA 单链可变片段( scFv )与 MM 细胞表面的 BCMA 结合,激活 CAR - T细胞并释放细胞毒性细胞因子,杀伤肿瘤细胞。目前全球针对 BCMA靶点的 CAR-T 疗法在自身免疫性疾病赛道布局的项目已有很多,大多数处于临床早期,适应症以系统性红斑狼疮为主。
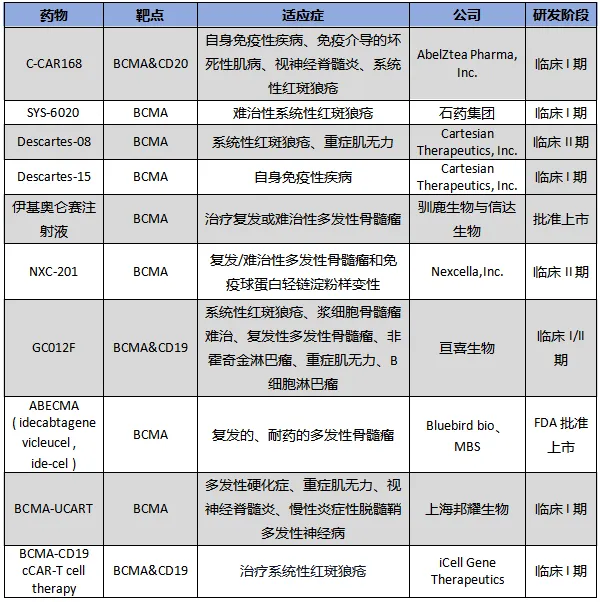
表
1.
靶向
BCMA CAR-T
疗法
ADC疗法
ADC是一种在提高单克隆抗体疗效的同时,也可以避免肿瘤晚期患者免疫细胞功能缺陷的一种免疫疗法,比传统抗肿瘤疗法更具有特异性,毒性不良反应更低,且选择性强,治疗效力更大。GSK2857916 是一种人源化 IgG1 抗 BCMA 单克隆抗体,与微蛋白聚合抑制剂 MMAF 偶联,通过 ADCC 和 ADCP 作用来促进表达 BCMA 的肿瘤细胞的细胞裂解 [5]。 2020年 8 月 5 日,美国食品药品监督管理局( FDA )批准了葛兰素史克( GSK )公司的 Blenrep ( belantamab mafodotin , GSK2857916 )上市。该药是一种靶向 B 细胞成熟抗原( BCMA )的抗体药物偶联物( ADC ),作为一种单药疗法,用于治疗先前已接受过至少 4 种疗法、且其疾病对至少一种蛋白酶体抑制剂 / 免疫调节剂 /CD38 单抗难治、在最后一次治疗中被证明疾病进展的复发或难治性多发性骨髓瘤( R/R MM )成人患者。
BsAb疗法
BsAb是一种很有前景的免疫治疗形式,与
MAb
比较,
BsAb
能够识别一种抗原的两个表位或两种抗原。
Pacanalotamab (AMG 420
;
BI-836909)
是一种双特异性
T
细胞接合剂
(BiTE)
,靶向
BCMA
和
CD3ɛ
,已针对
RRMM
患者进行了研究。
BiTE®
分子是融合蛋白,由具有独特抗原特异性的单链可变片段
m
(
scFv
)组成。
Pacanalotamab
会将
T
细胞重定向到细胞表面的
BCMA
表达细胞。可对人多发性骨髓瘤
(MM)
细胞系进行
T
细胞重定向裂解。
2024
年
6
月
25
日,强生宣布,其靶向
BCMA/CD3
的双抗特立妥单抗注射液(
Teclistamab
,商品名:泰立珂)正式获得国家药品监督管理局(
NMPA
)批准,用于治疗多发性骨髓瘤,也是中国首个获批上市的
BCMA/CD3
双特异性抗体。
BCMA/CD3
的双抗原理:能同时靶向
T
细胞
CD3
和
MM
细胞
BCMA
的
IgG4
双抗,其可将
CD3+T
细胞重新定向到表达
BCMA
的骨髓瘤细胞,以诱导针对靶细胞的细胞毒作用。
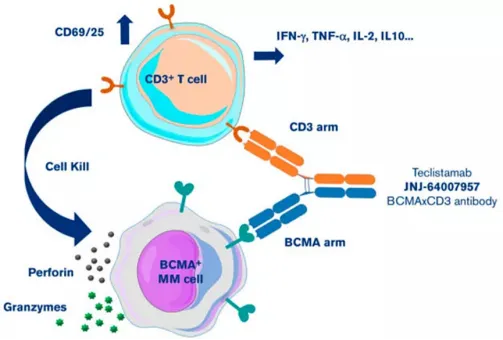
图 3. BCMA/CD3 双特异性抗体原理
BAFF是一种
B
细胞活化因子,它是肿瘤坏死因子配体超家族成员
13B
(
TNFSF13B
,
CD257
),也称为
BLyS
。它是一种
II
型跨膜蛋白,有
285
个氨基酸,存在一个
N
端胞外区,跨膜区,
C
端胞内区。膜结合形式的
BAFF
通过蛋白水解裂解加工为可溶性形式。它有三种受体:
BAFFR
(
TNFRSF13C
)、
TACI
(
TNFRSF13CB
)和
BCMA
(
TNFRSF17
),其中与
BAFFR
的作用最强,
BAFF
通过
BAFFR
受体作用支持成熟的未激活
B
细胞的存活。
BAFF
参与了人类许多自身免疫性疾病的发病机制。当
BAFF
过量表达时,会诱发多发性骨髓瘤的产生,而它的缺乏会导致机体免疫功能低下,引起一些免疫缺陷病的产生。
增殖诱导配体(
Aproliferation Inducingligand,
APRIL
,也称为
CD256
,
TNFSF13
)是肿瘤坏死因子家族的成员,在多种肿瘤组织中有高表达,能促进肿瘤细胞增殖,防止肿瘤细胞受
CD95L
、
FasL
等诱导的凋亡;调节体液免疫;并在
T
、
B
淋巴细胞的成熟和活化中起一定作用。
APRIL
作为
BCMA
的一个重要的配体,与
BCMA
的另一配体
BAFF
有着
30%
的序列同源性,却与它相比有着更高的亲和力与
BCMA
相互作用。
APRIL
与几种涉及自身反应性
B
细胞的人类自身免疫性疾病有关,包括系统性红斑狼疮
(SLE)
、
Sjagren Syndrome (SS)
、
IgA
肾病
(IgAN)
和类风湿性关节炎
(RA)
。因此,
APRIL
与肿瘤的发生、发展以及免疫系统的调节有密切关系。
从分子机制来看, BAFF和 APRIL 均可与骨髓瘤细胞表面的 TACI 及 BCMA 受体结合,其中 BAFF 还能与第三种受体 BAFF-R 相互作用 [6]。配体与 BCMA结合后, MM 细胞中多个生长和存活信号级联被激活,最常见的是 NF-κβ , RAS/MAPK 和 PI3K-PKB/Akt 信号通路。导致抗凋亡蛋白上调以及细胞粘附分子、血管生成因子和免疫抑制分子的产生 [1]。
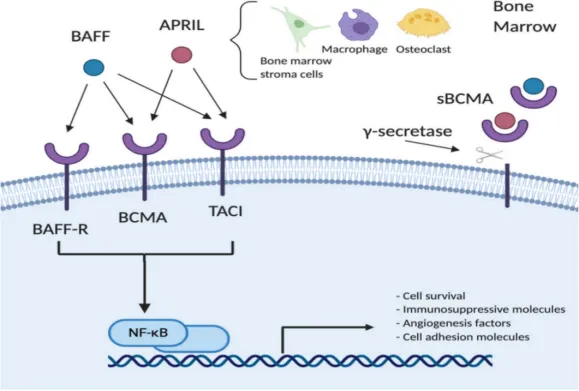
图 4. BCMA信号通路
迈杰医学蛋白平台具有丰富的生物标志物检测方法开发经验以及临床检测服务经验。当前,迈杰医学已完成了 sBCMA方法学全验证,包括:标准曲线重现性,批内 / 批间准确度和精密度,灵敏度,线性稀释,加标回收率和钩状效应,溶血和高脂验证,平行性,冻融稳定性、短期稳定性以及长期稳定性等验证参数。部分验证参数结果见下表。
表 2. sBCMA 验证参数
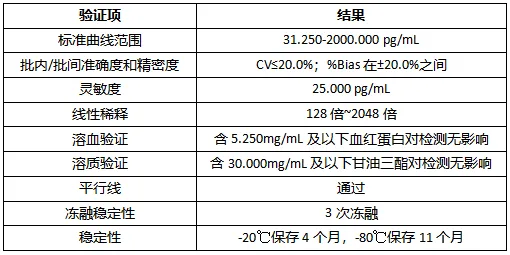
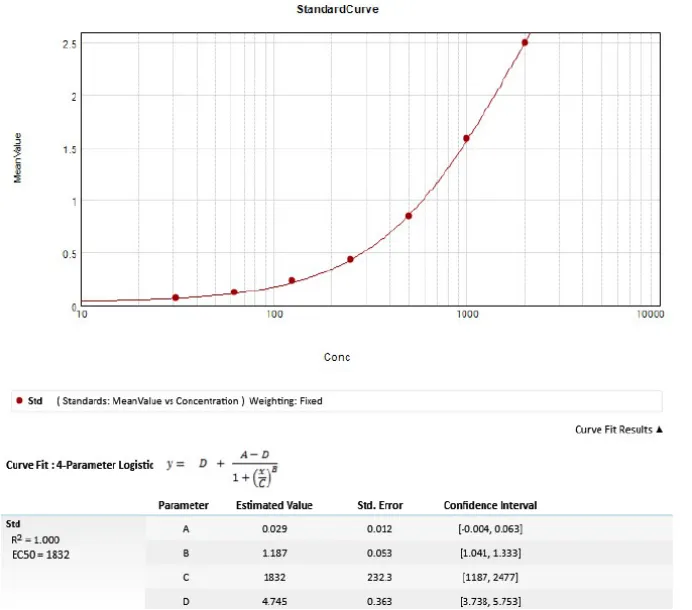
图 5 . 标准曲线拟合
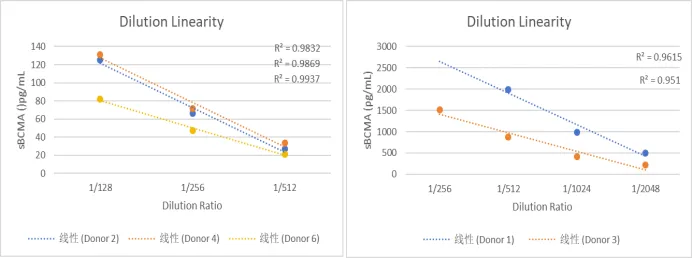
图 6 . 线性稀释
参考文献
[1] Yu , B., Jiang, T. & Liu, D. BCMA-targeted immunotherapy for multiple myeloma. J Hematol Oncol, 2020, 13, 125 .
[2] Laurent, S. A., Hoffmann, F. S., Kuhn, P. H., et al. γ-Secretase directly sheds the survival receptor BCMA from plasma cells. Nature communications, 2015, 6, 7333.
[3]
李燕娟
,张连生
,
李莉娟
.
多发性骨髓瘤单克隆抗体疗法、靶向
B细胞成熟抗原疗法研究进展
[J]
.医学研究杂志
,
2024,
52
(2) .
[4]
王珺
,刘爱春
.
多发性骨髓瘤的免疫治疗研究进展
[J] .
现代肿瘤医学
, 2022, 30(12) : 2263 - 2267.
[5]
Trudel S, Lendvai N, Popat R, et al. Targeting B - cell maturation antigen with GSK2857916 antibody - drug conjugate in relapsed or refractory multiple myeloma ( BMA117159 ) : a dose escalation and expansion phase 1 trial[ J] . Lancet Oncology, 2018, 19(12) : 1641 -1653.
[6] Hanley N. Abramson. B-Cell Maturation Antigen (BCMA) as a Target for New Drug Development in Relapsed and/or Refractory Multiple Myeloma[J]. Int. J. Mol. Sci. 2020, 21, 5192.