从迈谱康的临床试验数据显示:
非小细胞肺癌(1033例,其中非鳞状743例)样本中,在阳性阈值TC≥1%时,E1L3N与28-8的比对总符合率达到97.77%;
食管鳞癌(1029例)样本中,在阳性阈值CPS≥1时,E1L3N与22C3的比对总符合率达到95.72%;
胃癌(794例)样本中,在阳性阈值CPS≥5时,E1L3N与22C3的比对总符合率达到94.71%。
如下图 1显示, E1L3N 与 22C3 、 28-8 染色表现在同一趋势线下,而如图 2 显示, E1L3N 阳性的人群和 22C3 阳性人群接受帕博利珠单抗治疗后生存曲线几乎完全重合,体现出不同抗体药效学的相似性。
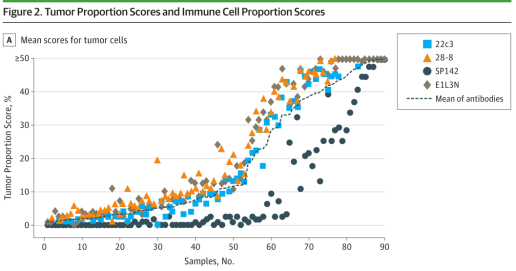
图 1. PD-L1不同克隆号抗体的染色评分表现 [1]
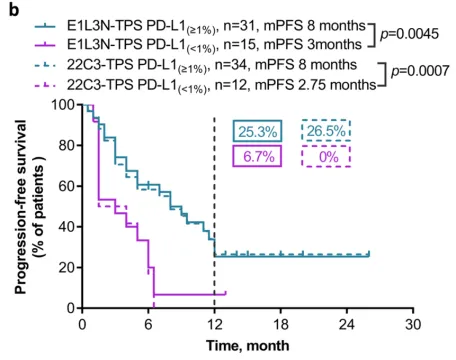
图 2. E1L3N与 22C3 指导帕博利珠单抗的疗效相似性 [2]
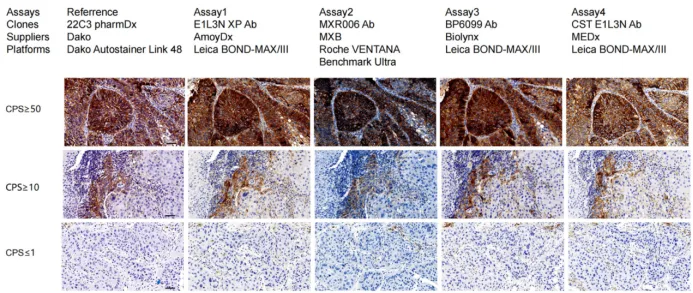
图 3. 参与食管鳞癌 PD-L1一致性研究的各抗体染色表现 [3]
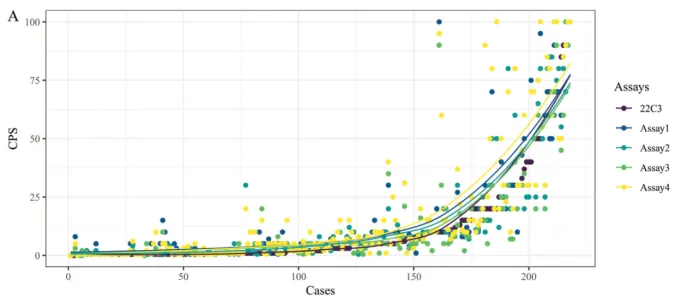
图 4. 各抗体 CPS评分表现 [3]
目前国内食管鳞癌免疫一线治疗方案多达8种,其中仅斯鲁利单抗联合方案需要限定PD-L1(E1L3N,CPS≥1)阳性人群。那么在真实世界中,这些方案对于PD-L1阴性人群的治疗是否不及预期?我们来看下专家的讨论结果。
去年9月,在美国食品药品管理局(FDA)的肿瘤药物咨询委员会(ODAC)会议上,讨论了对于不可切除或转移性ESCC患者一线使用抗PD-1抗体治疗时,PD-L1表达水平对其风险效益的影响。会议指出,ESCC的治疗批准在先前是不考虑PD-L1状态的,但已有多项试验显示:治疗效果似乎由PD-L1表达水平所影响,在PD-L1≥1的患者中风险效益更显著,而 对于PD-L1<1的患者,使用免疫检查点抑制剂可能使其面临毒性风险而无明确的获益潜力(图5 )。

图 5. FDA关于 ESCC 进行 PD-L1 评价的建议
迈杰医学的PD-L1检测试剂盒(克隆号E1L3N)在多个癌种中均体现出与进口抗体的高度一致性,同时具有相似的药效学数据。另外,在食管鳞癌多中心研究中,其凭借和22C3染色高度一致,并具有略高的灵敏度,在众多国产抗体中脱颖而出。目前该试剂盒具备以下特点:
双适应症伴随诊断——非鳞状非小细胞肺癌(纳武利尤单抗)、食管鳞状细胞癌(斯鲁利单抗)
专家共识推荐——《非小细胞肺癌PD-L1表达临床检测中国专家共识(2023版)》推荐检测抗体
多癌种应用——经多中心验证,在胃、头颈、宫颈等癌种与进口抗体高度一致
多平台适配——经验证可在Leica及多种国产免疫组化仪器适配使用
新适应症注册——胃癌适应症注册中,PD-L1判读软件已上市
参考文献
[1] A Prospective, Multi-institutional, Pathologist-Based Assessment of 4 Immunohistochemistry Assays for PD-L1 Expression in Non-Small Cell Lung Cancer. JAMA Oncol. 2017 Aug 1;3(8):1051-1058.
[2] Validation of E1L3N antibody for PD-L1 detection and prediction of pembrolizumab response in non-small-cell lung cancer. Commun Med (Lond). 2022 Nov 1;2(1):137.
[3] Concordance between four PD-L1 immunohistochemical assays and 22C3 pharmDx assay in esophageal squamous cell carcinoma in a multicenter study. J Natl Cancer Cent. 2023 Nov 30;4(2):162-168.