
图1.FDA官网来源[1]
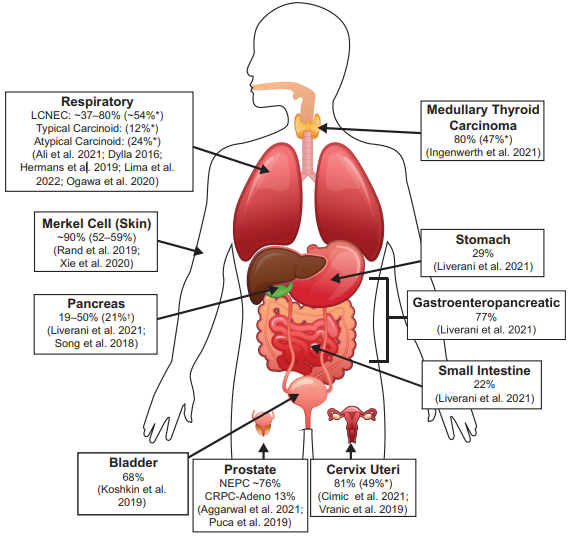
图2.DLL3在不同类型癌症组织中的表达[3]
截止发文,全球仅一款DLL3药物-塔拉妥单抗-获批(国内尚无获批),此药获批是基于DeLLphi-304研究,这是一项多中心、随机、开放标签的临床试验,入组的是接受过铂类化疗(可伴随或不伴随PD-1/PD-L1抑制剂)后病情进展的小细胞肺癌患者。共509名患者按1:1被随机分到两个组:一组接受塔拉妥单抗治疗,另一组接受研究者选择的标准化疗方案。研究结果发现:
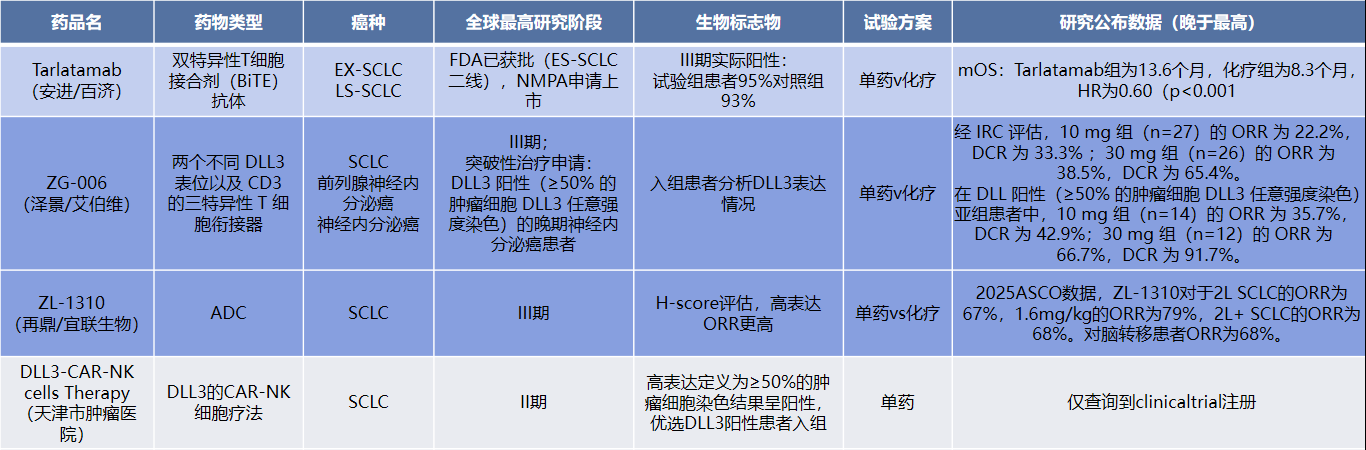
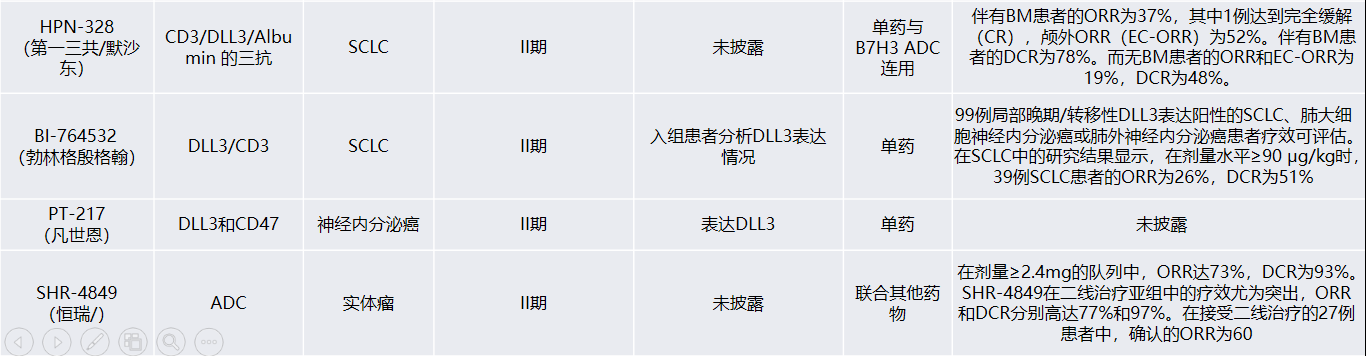
作为国内领先的转化医学中心实验室,我司拥有丰富的药企临床试验生物标志物检测经验。当前,迈杰转化医学与药企联合开发针对适应症NEC ,靶向DLL3的伴随试剂盒,采用同步开发的注册路径,已成功将该产品应用于药物关键III期临床试验入组筛选CTA使用。
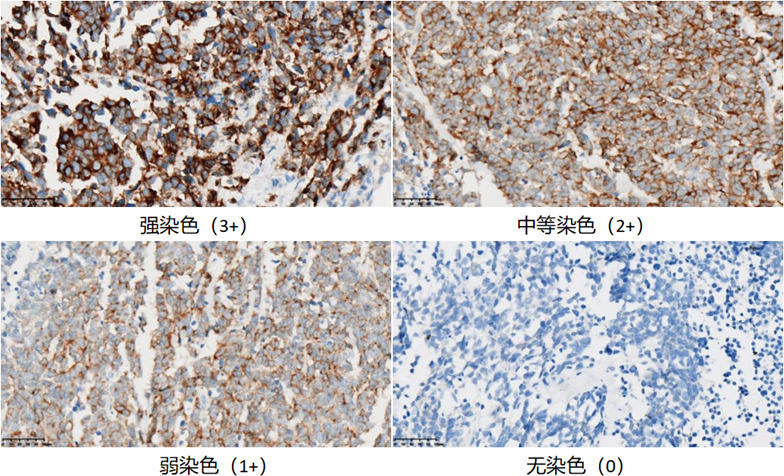
图4.迈杰DLL3检测试剂盒在DLL3不同表达程度肿瘤组织上的染色
迈杰转化医学病理中心可以提供从靶点发现、临床前研究到伴随诊断开发与临床样本检测的全流程、一体化病理解决方案。中心配备了常规IHC、多重免疫荧光(mIF)、RNA
原位杂交(RNAScope)及FISH/CISH等尖端技术平台,并依托Leica、
Ventana、Dako、Akoya等国际一流全自动化设备,结合HALO®人工智能图像分析系统,确保数据精准、客观、全程可溯源。
凭借丰富的项目经验,我们已成功验证超过200种生物标志物,为300余个药物靶点建立了成熟检测方法,覆盖 500多种适应症,并在肿瘤微环境分析、肿瘤免疫评估及多靶点共标 Panel开发等前沿领域积累了深厚洞见。在自主研发方面,成果显著:已获得多张NMPA注册证(包括PD-L1伴随诊断试剂)及多项CE认证,覆盖肺癌、胃癌、乳腺癌等高发癌种。
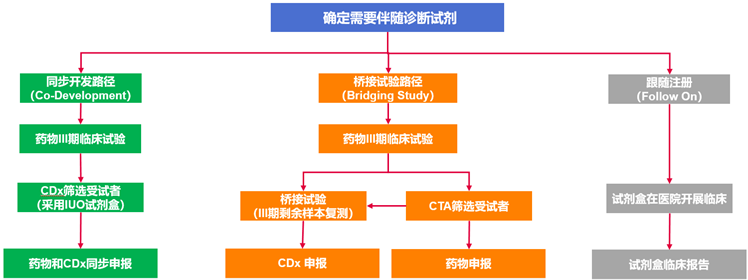
图5. 迈杰转化医学伴随诊断试剂开发和注册路径
📞 业务 咨询电话:400-007-1121
参考文献
[1]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-traditional-approval-tarlatamab-dlle-extensive-stage-small-cell-lung-cancer
[2]Pharmaceutics. 2025 Apr 16;17(4):520. doi: 10.3390/pharmaceutics17040520.
[3]Oncologist. 2022 Nov 3;27(11):940-951. doi: 10.1093/oncolo/oyac161.
[4]Lung Cancer. 2020 Sep:147:237-243. doi: 10.1016/j.lungcan.2020.07.026. Epub 2020 Jul 27.
[5]Lung Cancer. 2025 Sep:207:108723. doi: 10.1016/j.lungcan.2025.108723. Epub 2025 Aug 23.
[6]Endocr Pathol. 2025 Mar 28;36(1):9. doi: 10.1007/s12022-025-09854-3.
[7]N Engl J Med. 2025 Jul 24;393(4):349-361. doi: 10.1056/NEJMoa2502099. Epub 2025 Jun 2.
[8]ESMO2025 2773P.